Dicas de estudo - 6º ano
H2O é a fórmula da água, indicando que ela é composta por um átomo de oxigênio e dois de hidrogênio.
Encontramos, na natureza, essa substância de suma importância para a sobrevivência dos seres vivos, no estado sólido em geleiras de regiões bastante frias, bem assim no estado de vapor formando as nuvens e a atmosfera, ou na forma líquida em rios, mares, lagos, entre outros.
Nas condições normais de temperatura e pressão, a forma mais encontrada no mundo, é a água em estado líquido, em decorrência à sua estrutura química e ao seu ponto de ebulição bastante alto, fervendo somente aos 100ºC.
A água é um solvente
No ambiente é muito difícil encontrar água pura, em razão da facilidade com que as outras substâncias se misturam a ela. Mesmo a água da chuva, por exemplo, ao cair, traz impurezas do ar nela dissolvidas.
Uma das importantes propriedades da água é a capacidade de dissolver outras substâncias. A água é considerada solvente universal, porque é muito abundante na Terra e é capaz de dissolver grande parte das substancias conhecidas.
Se percebermos na água cor, cheiro ou sabor, isso se deve a substâncias (líquidos, sólidos ou gases) nela presentes, dissolvidas ou não.
As substâncias que se dissolvem em outras (por exemplo: o sal) recebem a denominação de soluto. A substância que é capaz de dissolver outras, como a água, é chamada de solvente. A associação do soluto com o solvente é uma solução.
Tensão superficial
Essa força de atração entre as moléculas possibilita a existência de um fenômeno chamado de tensão superficial, que aparenta ser uma película fina na superfície da água, formada pelas ligações de hidrogênio (coesão) entre as moléculas.
Por causa dessa característica, insetos conseguem pousar sob a água sem afundar. A água tem uma tensão superficial maior que dos outros líquidos.

massa líquida está em constante movimento entre os continentes, os oceanos e a atmosfera, formando o ciclo da água.
A pressão nos líquidos
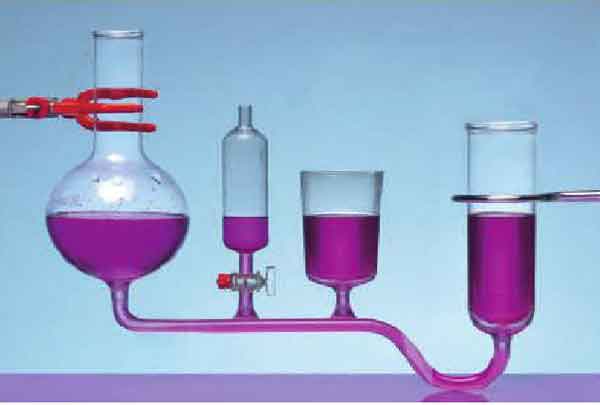
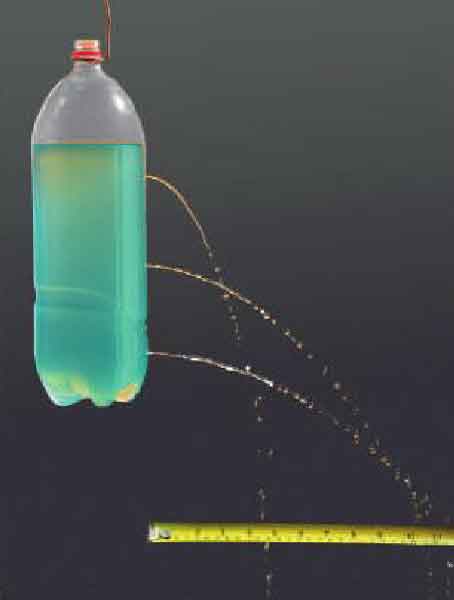 E no caso dos líquidos, como compreender os efeitos da pressão? Observe a fotografia ao lado. Nesse modelo, utilizando uma garrafa PET usada para refrigerantes, vemos que, quanto menor a altura da coluna de água dentro da garrafa, menor é a intensidade com que o jato de água sai da garrafa.
E no caso dos líquidos, como compreender os efeitos da pressão? Observe a fotografia ao lado. Nesse modelo, utilizando uma garrafa PET usada para refrigerantes, vemos que, quanto menor a altura da coluna de água dentro da garrafa, menor é a intensidade com que o jato de água sai da garrafa.
A pressão da água no nível do orifício depende da altura da coluna de água sobre ele: quanto maior a altura da coluna de liquido, maior será a pressão exercida. O alcance do jato de água vai diminuindo à medida que a altura da coluna de água vai diminuindo.
Os efeitos da pressão nos líquidos estão relacionados, por exemplo, com a construção de submarinos e com a construção de barragens de represas.
Como os submarinos se deslocam em diferentes profundidades nos mares e oceanos, é preciso que sejam construídos de modo a suportar grandes pressões de água. Por isso são construídos com estruturas altamente resistentes.
Princípio dos vasos comunicantes:
Observe, na ilustração abaixo, dois tubos (A e B) ligados entre si e a válvula que permite a comunicação entre eles.
Com a válvula fechada, você pode observar que, no tubo A, a altura da coluna de água em relação ao fundo do tubo é maior que no tubo B.
Esse fenômeno ocorre sempre que houver tubos de quaisquer formas e tamanhos interligados. Se você colocar um líquido em um dos tubos, ele irá se distribuir por todos os outros, atingindo o mesmo nível. Esse é o princípio dos vasos comunicantes.
O ciclo da água
Como ocorre
A evaporação das massas líquidas e a evapotranspiração da vegetação transferem umidade para a atmosfera, a qual se condensa, forma nuvens e volta para a superfície em forma de neve, chuva, granizo ou neblina.
Parte dessa água infiltra-se no solo e alimenta os lençóis subterrâneos, que, por sua vez, dão origem a nascentes ou olhos-d’água, retomando o ciclo novamente.
O ciclo da água ocorre graças à energia solar que permite a mudança de estado físico. A água se evapora das superfícies aquáticas e terrestres, formando as nuvens. Condensa-se e se precipita na forma de chuva, neve ou granizo.
No solo, a água pode atravessar os diversos horizontes (camadas) atraída pelas forças da gravidade, e atingir o lençol freático, de onde chega até um rio ou riacho. Parte da água precipitada pode ser retida pelo solo e absorvida pelas plantas, através do seu sistema radicular.
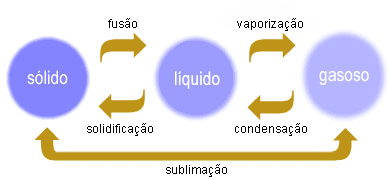
As passagens entre os três estados físicos (sólido, líquido e gasoso) têm o nome de mudanças de estado físico.
Observe o esquema a seguir e logo após leia as explicações sobre cada uma dessas mudanças.
Você já viu como num dia quente, um pedaço de gelo logo derrete depois de tirado do congelador?
Nesse caso, a água em estado sólido passa rapidamente para o estado líquido. Essa mudança de estado é conhecida como fusão.
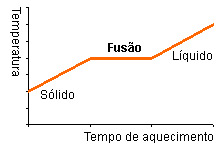
Fusão
Passagem, provocada por um aquecimento, do estado sólido para o estado líquido.
O aquecimento provoca a elevação da temperatura da substância até ao seu ponto de fusão. A temperatura não aumenta enquanto está acontecendo a fusão, isto é, somente depois que toda a substância passar para o estado líquido é que a temperatura volta a aumentar.
O ponto de fusão de uma substância é a temperatura a que essa substância passa do estado sólido para o estado líquido.
No caso da água o ponto de fusão é de 0ºC. Assim, o bloco de gelo permanecerá a 0ºC até todo ele derreter para só depois sua temperatura começar a se elevar para 1ºC, 2ºC etc.
Mas o contrário também acontece. Se quisermos passar água do estado líquido para o sólido, é só colocarmos a água no congelador. Essa mudança de estado é chamada solidificação.
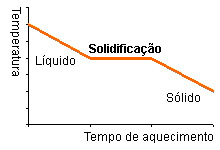
Solidificação
Passagem do estado líquido para o estado sólido, através de arrefecimento (resfriamento).
Quando a substância líquida inicia a solidificação, a temperatura fica inalterada até que a totalidade esteja no estado sólido, e só depois a temperatura continua a baixar.
Quando a substância líquida inicia a solidificação, a temperatura fica inalterada até que a totalidade esteja no estado sólido, e só depois a temperatura continua a baixar.
No caso da água o ponto de solidificação é de 0ºC. Assim, a água permanecerá a 0ºC até que toda ela congele para só depois sua temperatura começar a diminuir para -1ºC, - 2ºC etc.
Você já percebeu que, quando uma pessoa está cozinhando, ela tem que tomar cuidado para que a água não suma da panela e a comida queime e grude no fundo? Mas para onde vai a água?
A água passa para o estado gasoso: transforma-se em vapor, que não pode ser visto. A passagem do estado líquido para o estado gasoso é chamada vaporização.
Vaporização
Passagem do estado líquido para o estado gasoso, por aquecimento.
Se for realizada lentamente chama-se evaporação, se for realizada com aquecimento rápido chama-se ebulição.
Durante a ebulição a temperatura da substância que está a passar do estado líquido para o estado gasoso permanece inalterada, só voltando a aumentar quando toda a substância estiver no estado gasoso.
Se for realizada lentamente chama-se evaporação, se for realizada com aquecimento rápido chama-se ebulição.
Durante a ebulição a temperatura da substância que está a passar do estado líquido para o estado gasoso permanece inalterada, só voltando a aumentar quando toda a substância estiver no estado gasoso.
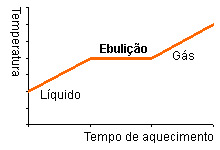
O ponto de ebulição de uma substância é a temperatura a que essa substância passa do estado líquido para o estado gasoso.
No caso da água o ponto de ebulição é de 100ºC. Assim toda a água permanecerá a 100ºC até toda ela tenha evaporado para somente depois sua temperatura começar a aumentar para 101ºC, 102ºC etc.
A água pode passar do estado de vapor para o estado líquido. É fácil observar essa passagem. Quantas vezes você já não colocou água gelada dentro de um copo de vidro fora da geladeira? Depois de um tempo, a superfície do lado de fora fica molhada, não é mesmo?
As pequenas gotas de água se formam porque o vapor de água que existe no ar entra em contato com a superfície fria do copo e se condensa, isto é, passa para o estado líquido. Essa mudança de estado é chamada condensação, ou liquefação.
Condensação
Passagem do estado gasoso para o estado líquido, devido ao um arrefecimento (resfriamento).
Quando a substância gasosa inicia a condensação, a temperatura fica inalterada até que a totalidade esteja no estado líquido, e só depois a temperatura continua a baixar.
Quando a substância gasosa inicia a condensação, a temperatura fica inalterada até que a totalidade esteja no estado líquido, e só depois a temperatura continua a baixar.
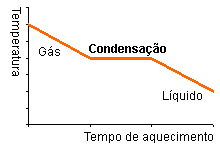
Um exemplo de condensação é o orvalho e a geada!
Às vezes, quando está frio, logo de manhã vemos que muitas folhas, flores, carros, vidraças e outros objetos que estão no ar livre ficam cobertos de gotas de água, sem que tenha chovido: é o orvalho.

O orvalho se forma quando o vapor de água presente no ar se condensa ao entrar em contato com superfícies que estão mais frias que o ar. Se a temperatura estiver muito baixa, a água pode congelar sobre as superfícies frias, formando uma camada de gelo: é a geada, que pode causar prejuízos às plantações, já que o frio pode destruir folhas e frutos.

Sublimação
Passagem direta de uma substância do estado sólido para o estado gasoso, por aquecimento, ou do estado gasoso para o estado sólido (cristalização). Ex. Gelo seco, naftalina.

Naftalina



Comentários
Postar um comentário